FX classix
Principali caratteristiche
Ottimizzazione del flusso ematico
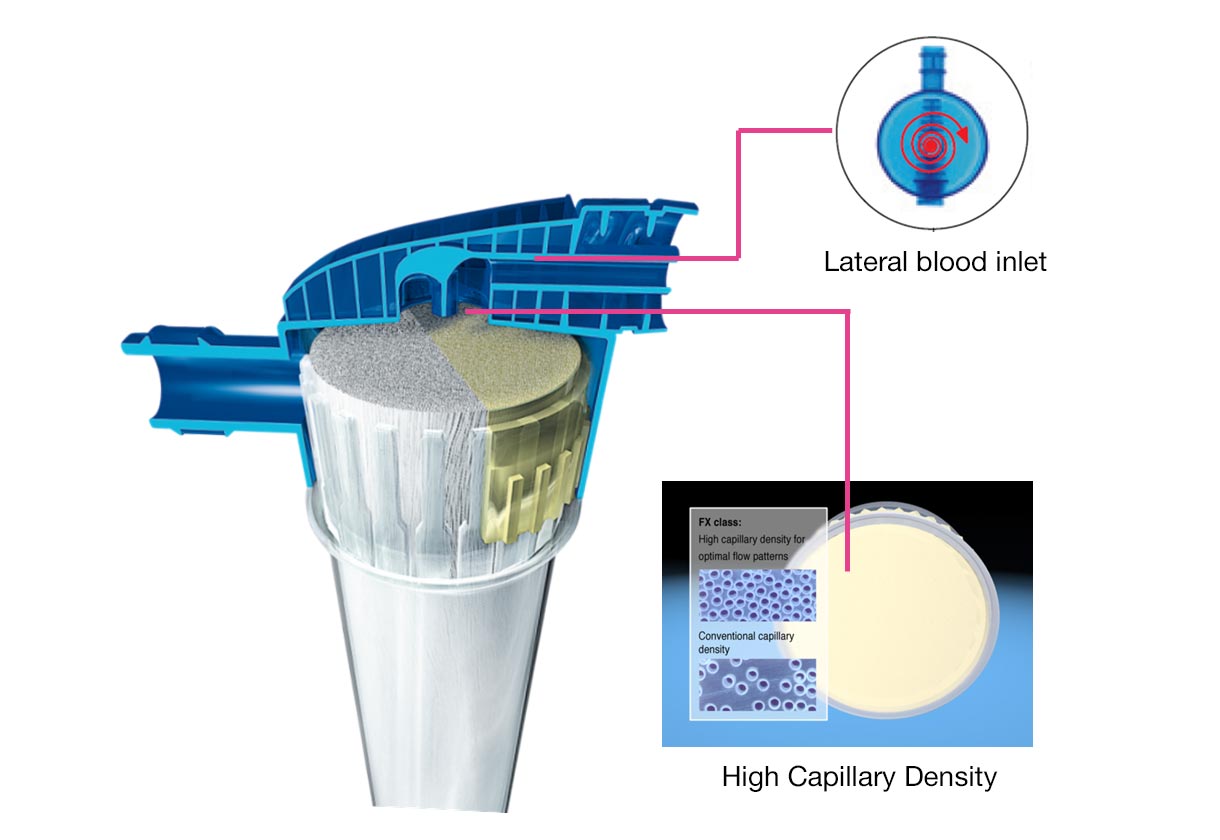
- L’ ingresso laterale per il sangue fornisce un flusso ematico omogeneo nell'ingresso del dializzatore, prevenendo zone di ristagno. Il design riduce al minimo il rischio di piegature, contribuendo a migliorare la sicurezza
- Un'alta densità dei capillari porta ad una disposizione più uniforme delle fibre.Questo garantisce una distribuzione omogenea del flusso ematico in ingresso a ciascuna fibra
Omogeneità del flusso dialisato per clearance superiori
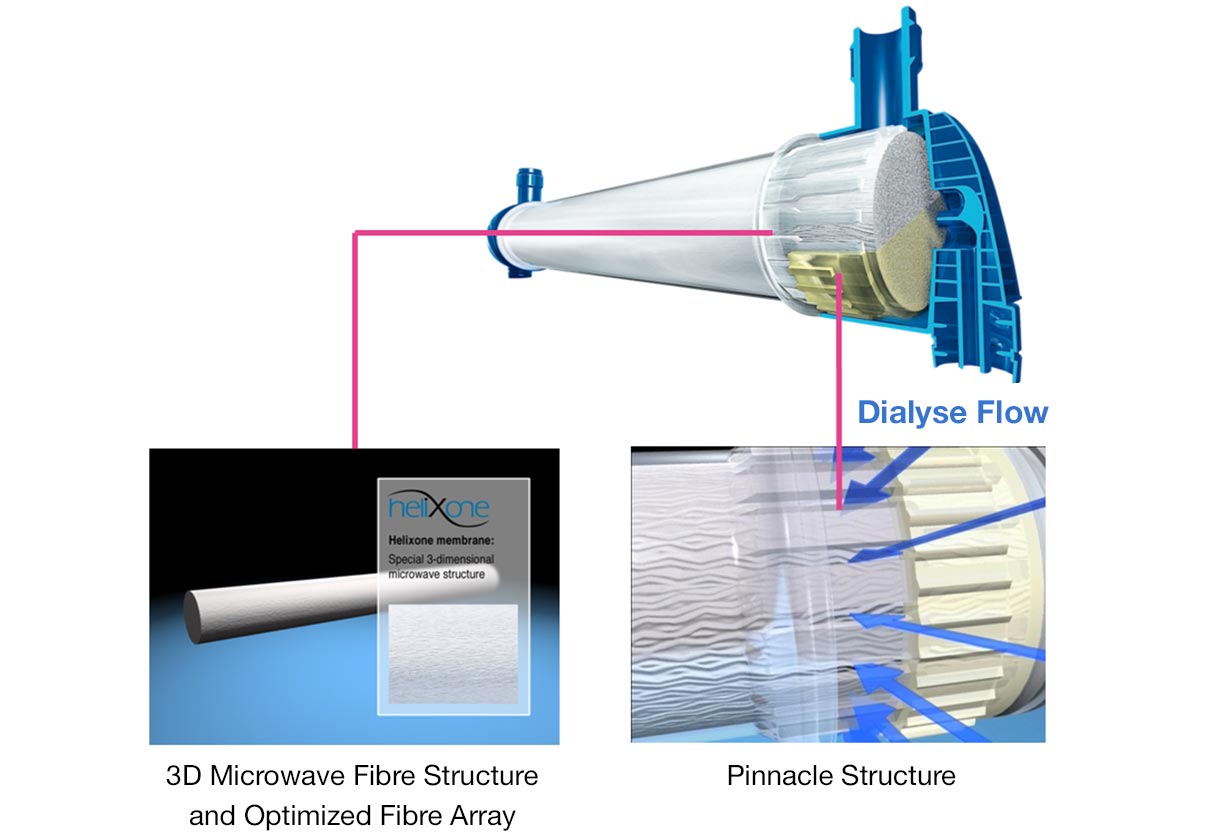
- La forma a guglia della struttura in polipropilene insieme alla tecnologia adottata per il potting garantisce l’uniformità del flusso radiale del dialisato attorno a ciascuna fibra del fascio
- L'ondulazione delle fibre impedisce l’incanalamento del dialisato, migliorando le prestazioni complessive del dializzatore. La maggiore densità del fascio di fibre insieme all'ondulazione dei capillari, consente un flusso uniforme del dialisato all'interno dell'intera sezione trasversale del fascio di fibre
Design dell’housing per FX-class®
Design FX-class®
Peso del dializzatore
| Il peso del dializzatore è un fattore cruciale non solo per gli aspetti logistici ma anche nella gestione dei rifiuti. L’housing dei dializzatori FX-class® è realizzato in polipropilene. Rispetto al comune policarbonato è molto più leggero, con il risultato che i dializzatori FX-class® pesano circa la metà rispetto alla maggior parte dei dializzatori. | |
|---|---|
| FX 60 classix | 107 g |
| FX CorDiax 60 | 107g |
Vantaggi della sterilizzazione INLINE a vapore
| Nessun residuo chimico | Nessuna sterilizzazione a raggi gamma - le radiazioni ionizzanti ad alta energia possono degradare ed alterare la composizione chimica dei materiali. |
| Bassi volumi di lavaggio | Tempi di preparazione minimi - poichè i dializzatori sono forniti già puliti, i tempi di lavaggio prima dell’uso risultano estremamente ridotti. |
| Minor lavaggio – Riduzione dei costi | Ridurre i volumi di lavaggio significa contenere tempi e costi di preparazione. |
Tecnologia
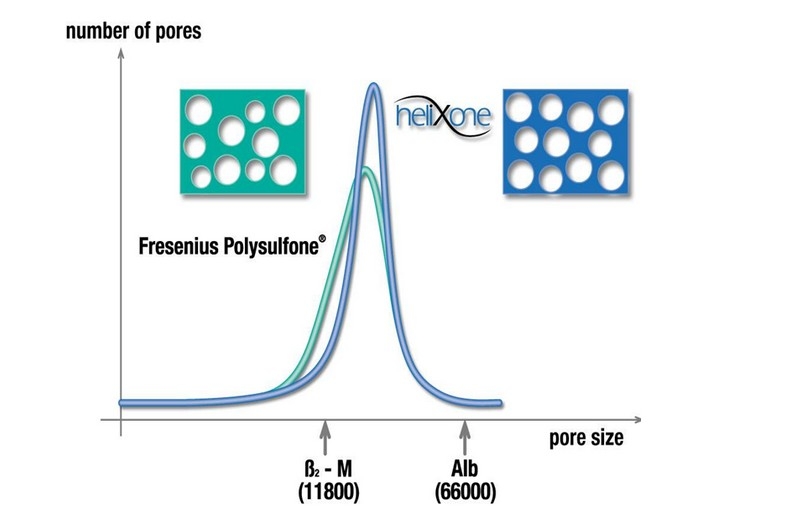
Migliori clearance grazie alle nanotecnologie
Pori convenzionali
Pori nella membrana Helixone®
Quando sono stati introdotti sul mercato i dializzatori FX-class®, era stata sviluppata un'innovativa tecnologia di filatura per la produzione della membrana in Helixone®. La cosiddetta tecnologia Nano Controlled Spinning (NCSTM) ha permesso la produzione ad alta definizione della struttura dei pori. Contrariamente ai pori convenzionali prodotti in precedenza, di forma irregolare, i pori sullo strato interno della membrana Helixone® sono lisci e cilindrici. Questo riduce la resistenza delle molecole quando attraversano la parete della membrana e ciò consente una maggiore rimozione.
Ottimizzazione dei pori attraverso la nanotecnologia
Tutte le membrane Helixone® ottimizzano le proprietà di sieving, in quanto la distribuzione della dimensione dei pori sulla superficie interna è stata ridotta rispetto alle membrane prodotte in precedenza, come nella serie F. La dimensione media dei pori è maggiore rispetto ai dializzatori serie F e la deviazione nelle dimensioni dei pori risulta inferiore. Ne risulta una migliore filtrazione per le medie molecole, quindi ad es. un più favorevole rapporto di sieving β2-m / albumina.
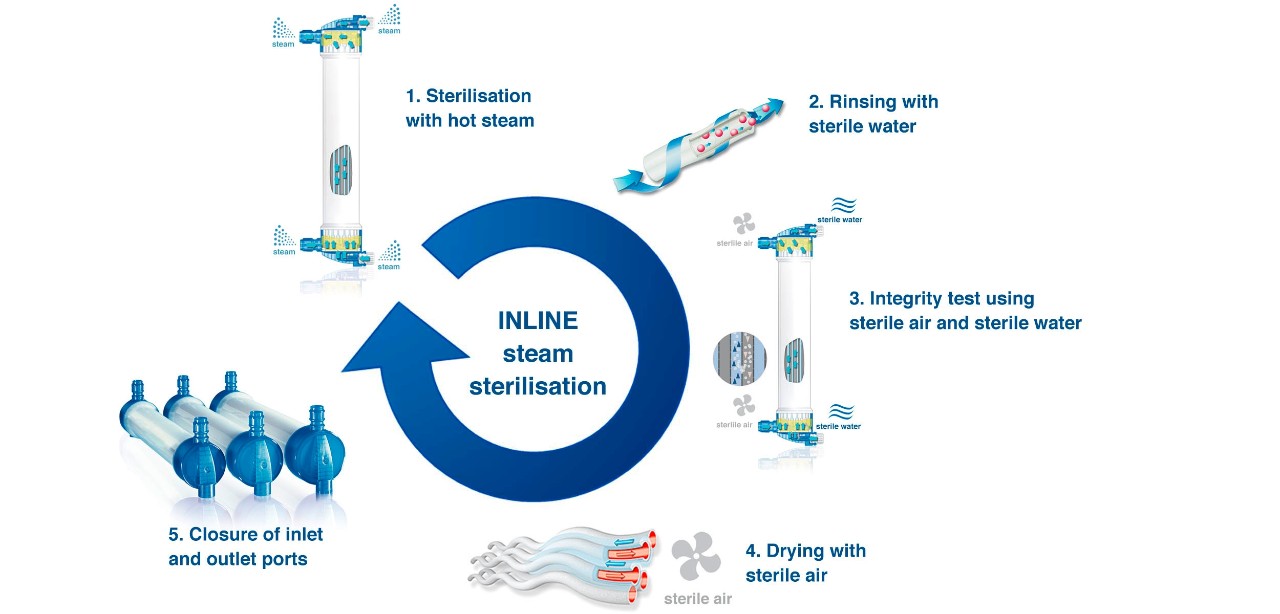
Sterilizzazione INLINE a vapore
Vantaggi del processo INLINE di sterilizzazione a vapore
- Dializzatori altamente puri, sterili e apirogeni senza alcun rischio potenziale derivante dalla presenza di residui chimici
- La biocompatibilità delle membrane non viene alterata dal processo di sterilizzazione
- Uso ottimizzato delle risorse grazie ai bassi volumi di lavaggio: sono necessari solo 500 mL
- Minore rischio di perdite ematiche e rottura delle fibre grazie alla verifica di integrità sul 100% delle fibre
- Dializzatori asciutti con rischio minimo di contaminazione da proliferazione microbica
Test di integrità delle fibre
Tutti i dializzatori devono superare il test di integrità. Durante il test, aria sterile viene spinta nel compartimento dialisato, mentre il compartimento ematico contiene acqua sterile. In presenza di perdite l’aria attraversa la membrana, generando bolle. Questo test di integrità riduce al minimo il rischio di rottura delle fibre e quindi il rischio di perdite ematiche.
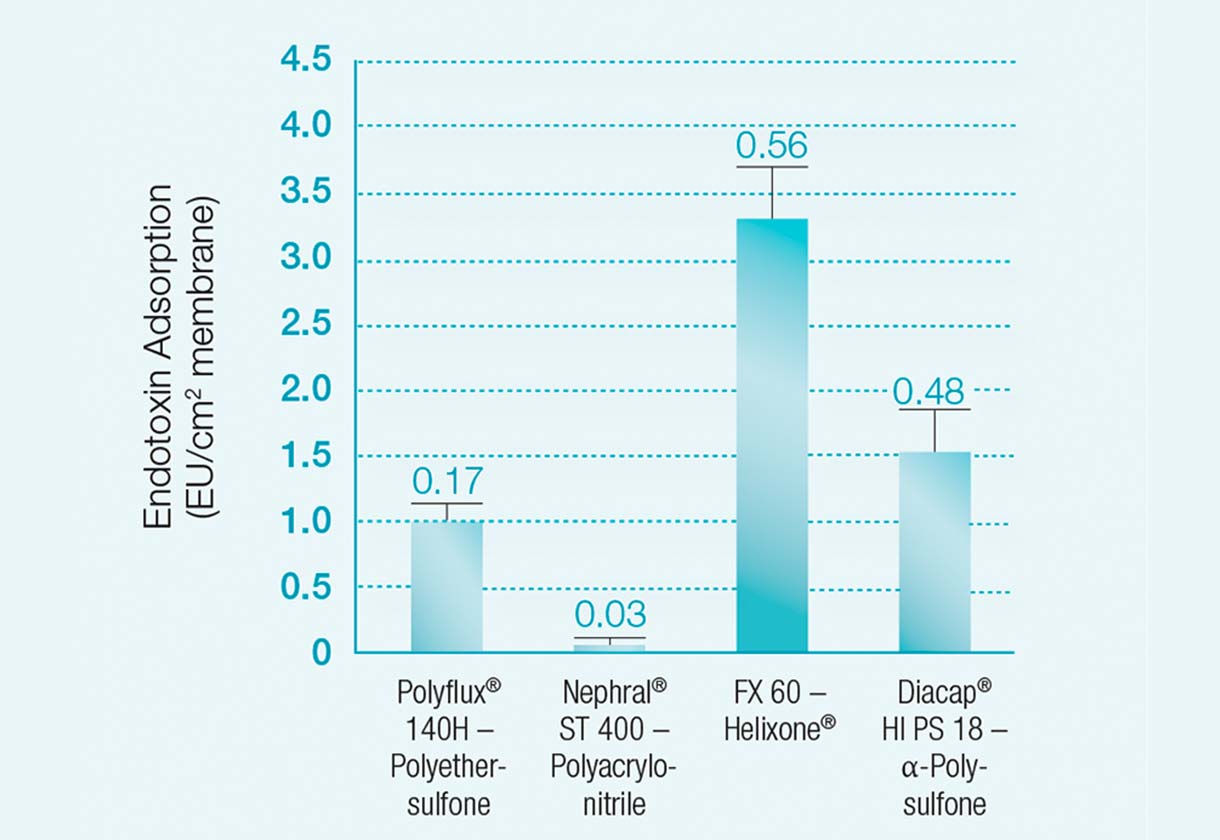
Elevata capacità di ritenzione delle endotossine della membrana Helixone®
Weber et al. (2003) hanno confrontato la capacità di adsorbimento endotossinica di diversi dializzatori.
La membrana Helixone® di un dializzatore FX 60 aveva una maggiore capacità di adsorbimento endotossinica rispetto a:
- Polyflux® 140H di Gambro - Polietersulfone (Poliammide S)
- Nephral® ST 400 di Gambro - Poliacrilonitrile (AN69ST)
- Diacap® HI PS 18 di B. Braun - Alpha-Polysulfone
Dati prestazionali
Dati sulle prestazioni
| Dializzatori FX classix ad alto flusso | FX 50 classix | FX 60 classix | FX 80 classix | FX 100 classix | |
|---|---|---|---|---|---|
| Clearance (QB = 300 mL/min) | Peso molecolare (Dalton) | ||||
| Citocromo c | 12 230 | 55 | 74 | 89 | 100 |
| Inulina | 5200 | 72 | 95 | 113 | 122 |
| Vitamina B12 | 1355 | 137 | 162 | 185 | 201 |
| Fosfati | 132 | 204 | 225 | 244 | 253 |
| Creatinina | 113 | 224 | 243 | 259 | 264 |
| Urea | 60 | 253 | 266 | 279 | 280 |
| Clearance (QB = 400 ml/min) | |||||
| Citocromo c | 12 230 | 76 | 92 | 105 | |
| Inulina | 5200 | 99 | 119 | 129 | |
| Vitamina B12 | 1355 | 175 | 202 | 222 | |
| Fosfati | 132 | 252 | 279 | 291 | |
| Creatinina | 113 | 277 | 300 | 309 | |
| Urea | 60 | 312 | 334 | 336 | |
| Coeficiente de ultrafiltración (ml/h x mm Hg) | 27 | 38 | 53 | 68 | |
| Coefficiente di sieving | |||||
| Albumina | 66,500 | < 0.001 | |||
| Mioglobina | 17,053 | 0.1 | |||
| β2-microglobulina | 11,731 | 0.7 | |||
| Inulina | 5,200 | 1 | |||
| Prestazioni in vitro: QD = 500 mL/min, QF = 0 mL/min, T = 37°C (ISO8637). Coefficiente di ultrafiltrazione: sangue umano, ematocrito 32 %, proteine totali 6 %. | |||||
| Membrana | Helixone® | ||||
| Metodo di sterilizzazione | Inline Steam | ||||
| Materiale housing | Polipropileno | ||||
| Materiale potting | Poliuretano | ||||
| Unità per confezione | 24 | ||||
| Superficie effettiva (m²) | 1.0 | 1.4 | 1.8 | 2.2 | |
| K0A Urea | 866 | 1,068 | 1,394 | 1,429 | |
| Volume ematico di riempimento (mL) | 53 | 74 | 95 | 116 | |
| Codice articolo | F00002385 | F00002386 | F00002387 | F00002388 | |
1 Weber V. et al., Blood Purification (2003); 21: 365.