HighVolumeHDF w standardzie.
Dializatory wysokoprzepływowe i niskoprzepływowe FX
Główne cechy
Promieniowy przepływ dializatu
- Kolczysta struktura obudowy polipropylenowej zapewnia równomierny przepływ dializatu wokół całej wiązki włókien
- Wysoka gęstość upakowania wiązki włókien i specjalna falista struktura włókien, aby uniknąć kanałowego przepływu dializatu
- Połączenie tych cech umożliwia stałą wydajność wszystkich dializatorów FX
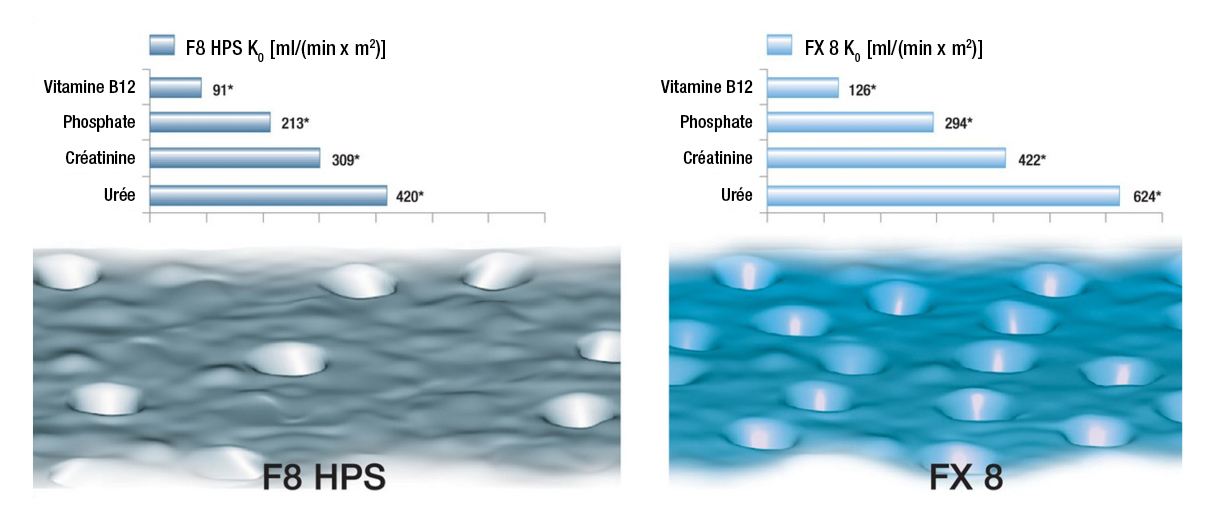
Optymalne wymiary włókien
- Zredukowana średnica wewnętrzna i grubość ścianki włókna zwiększają wewnętrzną filtrację i minimalizują opór dyfuzyjny
- W ten sposób uzyskuje się znaczny wzrost zarówno klirensu dyfuzyjnego, jak i konwekcyjnego, umożliwiając skuteczne usuwanie szerokiego spektrum toksyn mocznicowych
Technologia
Helixone® — zaawansowana membrana polisulfonowa
- Procedury wytwarzania membran w nanotechnologii (Nano Controlled Spinning Technology, NCS™) zapewniają Helixone® wysoce zdefiniowaną strukturę porów i ich rozmieszczenie w najbardziej wewnętrznym, oddzielającym obszarze membrany1,2
- W przeciwieństwie do konwencjonalnych porów, które były chropowate i nierówne, pory w wewnętrznej warstwie membrany Helixone® są gładkie i cylindryczne
- Zmniejsza to opór dla cząsteczek podczas przechodzenia przez pory i umożliwia lepsze usuwanie
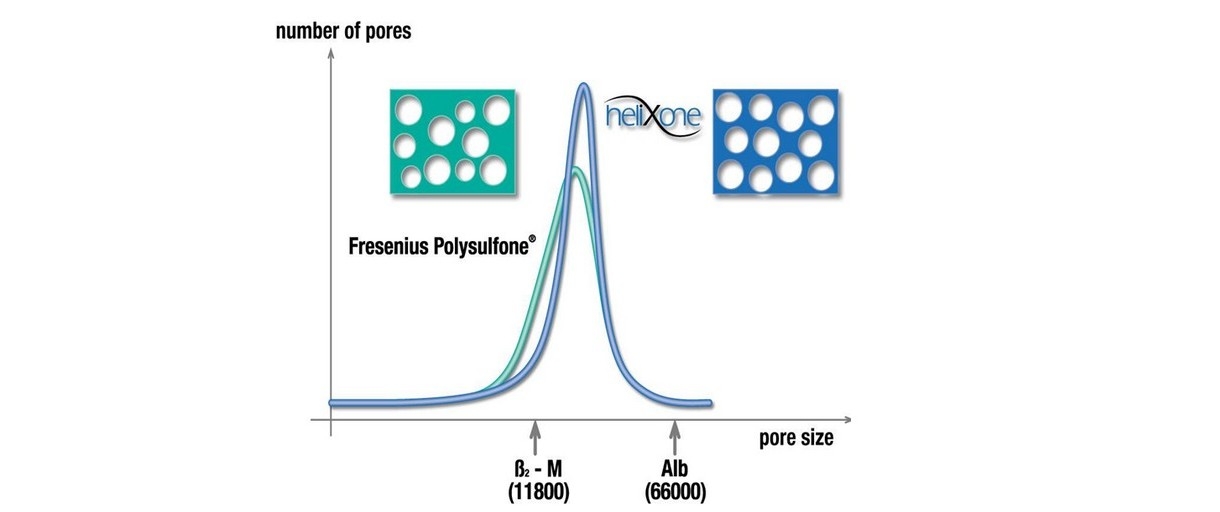
Helixone® została specjalnie zaprojektowana, aby spełnić wymagania zarówno w przypadku terapii o niskim, jak i wysokim przepływie:More even distribution of pores
- Bardziej równomierne rozmieszczenie porów
- Szacowany zwiększony średni rozmiar porów wynosi 1,8 nm (niski przepływ) i 3,3 nm (wysoki przepływ)
- Zwiększona wydajność na jednostkę powierzchni
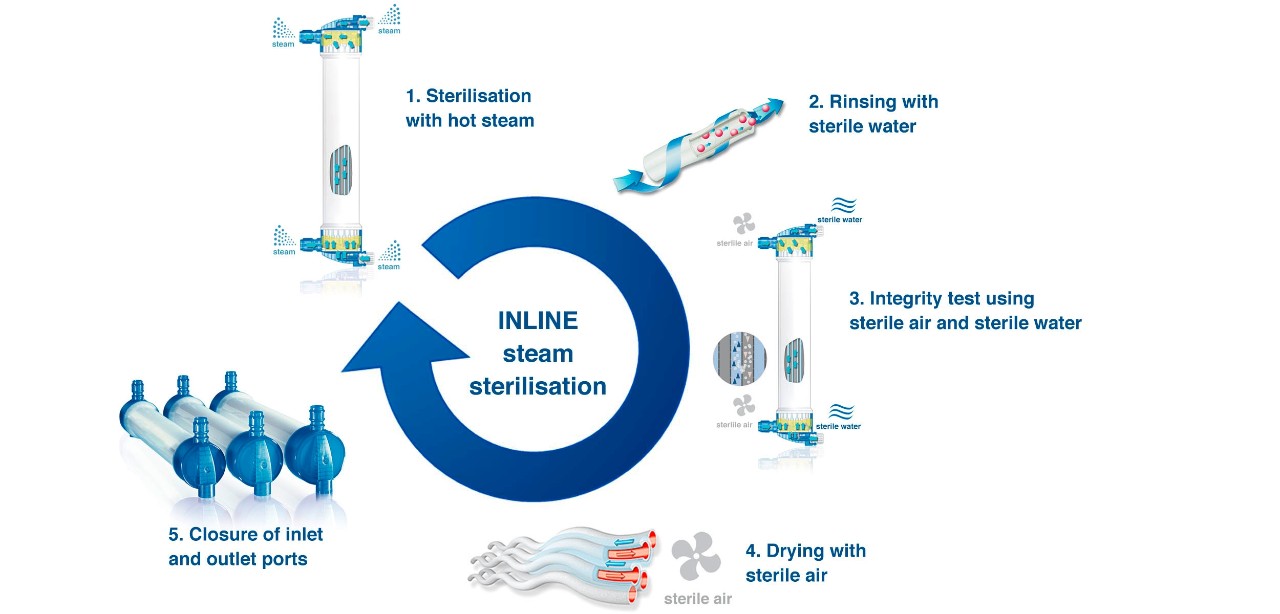
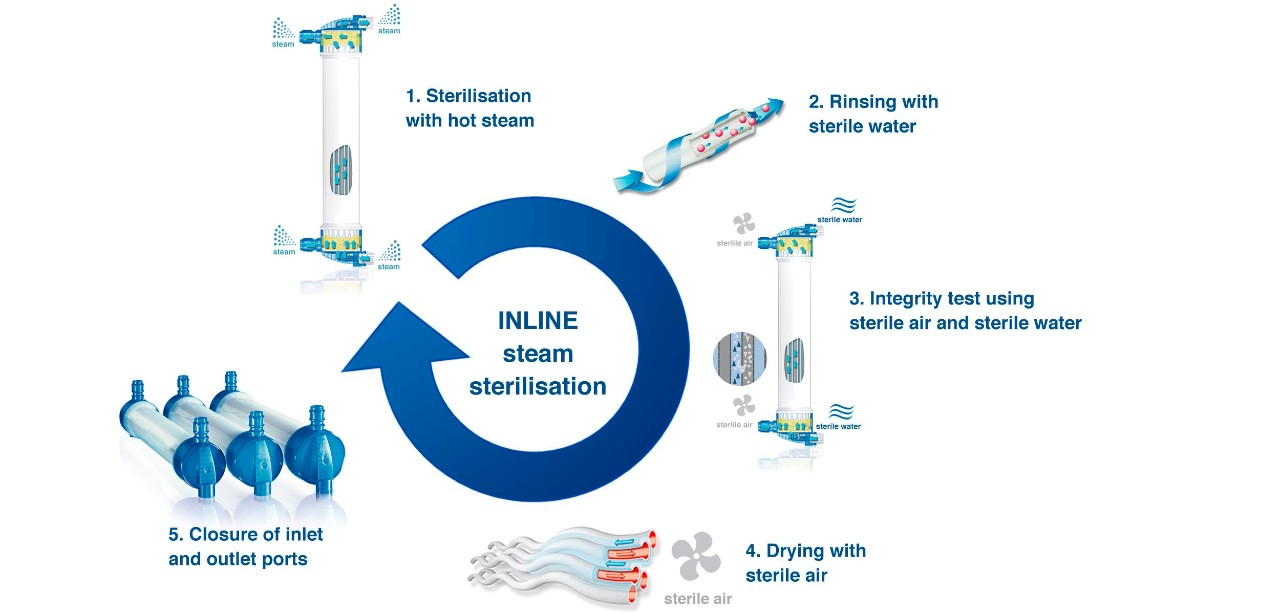
Sterylizacja parowa INLINE – gwarancja czystości
Bez pozostałości chemicznych. Niska objętość płukania. Niższe koszty.
Sterylizacja parowa INLINE – zalety
- Wysoce czyste, sterylne i wolne od pirogenów dializatory bez potencjalnie szkodliwych pozostałości po sterylizacji
- Sterylizacja nie ma wpływu na biozgodność membran
- Optymalne wykorzystanie zasobów dzięki niskim objętościom płukania: wymagane jest jedynie 500 ml
- Suche dializatory o zminimalizowanym ryzyku zanieczyszczenia w wyniku rozwoju mikroorganizmów
Dane dotyczące wydajności
Dializatory niskoprzepływowe FX
| Dializatory niskoprzepływowe FX | FX 5 | FX 8 | FX 10 | |
|---|---|---|---|---|
| Współczynnik ultrafiltracji (ml/h x mmHg) | 8 | 12 | 14 | |
| Klirens: QB: (200ml/min) | ||||
| Mocznik | 180 | 191 | 193 | |
| Kreatynina | 165 | 178 | 181 | |
| Fosforan | 141 | 160 | 170 | |
| Witamina B12 | 88 | 107 | 121 | |
| Klirens: QB: (300ml/min) | ||||
| Mocznik | 228 | 254 | 261 | |
| Kreatynina | 200 | 225 | 231 | |
| Fosforan | 164 | 194 | 210 | |
| Witamina B12 | 94 | 120 | 138 | |
| Klirens: QB: (400ml/min) | ||||
| Mocznik | 293 | 303 | ||
| Kreatynina | 252 | 260 | ||
| Fosforan | 213 | 233 | ||
| Witamina B12 | 126 | 146 | ||
| Dane wydajności in vitro uzyskano przyQD = 500ml/min: QF = 0ml/min; T=37°C (ISO8637) Współczynniki ultrafiltracji utrzymano przy użyciu ludzkiej krwi, Hct = 32%, zawartość białka 6% |
||||
| Powierzchnia efektywna (m²) | 1,0 | 1,4 | 1,8 | |
| Objętość zalewania krwią (ml) | 54 | 74 | 95 | |
| Materiał membrany | Helixone® | |||
| Materiał obudowy | Polipropylen | |||
| Pierścień oddzielający | Poliuretan | |||
| Metoda sterylizacji | Sterylizacja parowa INLINE | |||
| Zastosowanie | HD | |||
Dializatory wysokoprzepływowe FX
| Dializatory wysokoprzepływowe FX | FX 40 | FX 50 | FX 60 | FX 80 | FX 100 |
|---|---|---|---|---|---|
| Współczynnik ultrafiltracji (ml/h x mmHg) | 20 | 33 | 46 | 59 | 73 |
| Klirens: QB: (200ml/min) | |||||
| Mocznik | 170 | 189 | 193 | 197 | |
| Kreatynina | 144 | 170 | 182 | 189 | |
| Fosforan | 138 | 165 | 177 | 185 | |
| Witamina B12 | 84 | 115 | 135 | 148 | |
| Inulina | 54 | 76 | 95 | 112 | |
| Klirens: QB: (300ml/min) | |||||
| Mocznik | 250 | 261 | 276 | 278 | |
| Kreatynina | 210 | 230 | 250 | 261 | |
| Fosforan | 201 | 220 | 239 | 248 | |
| Witamina B12 | 130 | 155 | 175 | 192 | |
| Inulina | 81 | 104 | 125 | 142 | |
| Klirens: QB: (400ml/min) | |||||
| Mocznik | 303 | 362 | 331 | ||
| Kreatynina | 262 | 287 | 304 | ||
| Fosforan | 248 | 272 | 284 | ||
| Witamina B12 | 167 | 190 | 213 | ||
| Inulina | 109 | 133 | 152 | ||
| Dane wydajności in vitro uzyskano przyQD = 500ml/min: QF = 0ml/min; T=37°C (ISO8637) Współczynniki ultrafiltracji utrzymano przy użyciu ludzkiej krwi, Hct = 32%, zawartość białka 6% |
|||||
| Powierzchnia efektywna (m²) | 0,6 | 1,0 | 1,4 | 1,8 | 2,2 |
| Objętość wypełniania krwią (ml) | 32 | 53 | 74 | 95 | 116 |
| Materiał membrany | Helixone® | ||||
| Materiał obudowy | Polipropylen | ||||
| Pierścień oddzielający | Poliuretan | ||||
| Metoda sterylizacji | Sterylizacja parowa INLINE | ||||
| Zastosowanie | HD/HDF/HF | ||||
Hemodiafiltry FX
| Hemodiafiltry FX | FX 600 | FX 800 | FX 1000 |
|---|---|---|---|
| Współczynnik ultrafiltracji (ml/h x mmHg) | 52 | 63 | 75 |
| Klirens: QB: (200ml/min) QF: (0ml/min) | |||
| Mocznik | 196 | 198 | |
| Kreatynina | 184 | 190 | |
| Fosforan | 180 | 184 | |
| Witamina B12 | 141 | 149 | |
| Inulina | 101 | 110 | |
| Klirens: QB: (300ml/min) QF: (75ml/min) | |||
| Mocznik | 284 | 289 | 290 |
| Kreatynina | 262 | 271 | 280 |
| Fosforan | 254 | 262 | 269 |
| Witamina B12 | 199 | 209 | 211 |
| Inulina | 150 | 161 | 164 |
| Klirens: QB: (400ml/min) QF: (100ml/min) | |||
| Mocznik | 351 | 361 | 364 |
| Kreatynina | 313 | 328 | 343 |
| Fosforan | 301 | 313 | 325 |
| Witamina B12 | 229 | 241 | 244 |
| Inulina | 172 | 185 | 188 |
| Dane wydajności in vitro uzyskano przyQD = 500ml/min: T=37°C (ISO8637) Współczynniki ultrafiltracji utrzymano przy użyciu ludzkiej krwi, Hct = 32%, zawartość białka 6% |
|||
| Powierzchnia efektywna (m²) | 1,5 | 1,8 | 2,2 |
| Grubość ściany / średnica wewnętrzna (µm) | 35/210 | ||
| Objętość wypełniania krwią (ml) | 97 | 118 | 138 |
| Materiał membrany | Helixone® | ||
| Materiał obudowy | Polipropylen | ||
| Pierścień oddzielający | Poliuretan | ||
| Metoda sterylizacji | Sterylizacja parowa INLINE | ||
| Zastosowanie | HD/HDF | ||
Powiązane treści
1 Bowry, S.K.: Nano-controlled membrane spinning technology: Regulation of pore size, distribution and morphology of a new polysulfone dialysis membrane. In Hemodialysis Technology (eds: Ronco, C., La Greca, G.) Contributions to Nephrology, Vol. 137: 85-94 (2002)
2 Ronco, C., Nissenson, A.R.: Does nanotechnology apply to dialysis? Blood Purification 19: 347-352 (2001)