Medizinprodukte-Verordnung
Verordnung (EU) 2017/745
Die MDR wirft viele Fragen zu folgenden Aspekten auf:
Ihre Auswirkungen auf die ständige Verfügbarkeit der Produkte von Fresenius Medical Care
Einzelheiten zur Anwendbarkeit für Kunden und Nutzer unserer Medizinprodukte
Aufgrund des Umfangs und der Komplexität der neuen MDR wurden die neuen Anforderungen im Rahmen von Sonderprogrammen umgesetzt und von der Geschäftsführung in enger Abstimmung mit unserer benannten Stelle beaufsichtigt.
Die meisten Produkte unseres Portfolios sind bereits durch unser EU MDR Zertifikat abgedeckt. Weitergehend wird MDR Konformität und der komplette Übergang unserer MDD-zertifizierten Produkte durch etablierte globale Prozesse sichergestellt.
Der folgende Abschnitt enthält Fragen und Antworten zur Umsetzung der MDR durch Fresenius Medical Care und deren Folgen für Kunden und Nutzer unserer Medizinprodukte.
Fragen und Antworten
Erfüllt Fresenius Medical Care die MDR-Anforderungen?
Die Konformität des Qualitätsmanagementsystems von Fresenius Medical Care mit den geltenden MDR- Anforderungen wurde bei externen Audits durch die benannte Stelle im Jahr 2019 bewertet und bestätigt. Seitdem unterliegen wir regelmäßigen Überwachungs-/Rezertifizierungsaudits hinsichtlich der MDR-Konformität.
Eine ebenso wichtige Vorrausetzung für die Erteilung der MDR-Zertifizierung ist die Produktprüfung hinsichtlich der Konformität mit den Anforderungen der MDR. Nach erfolgreicher Beurteilung der entsprechenden Technischen Dokumentation durch die benannte Stelle wurden die erste Produktkategorien auf das MDR Zertifikat aufgenommen. Im Einklang mit den MDR-Übergangsbestimmungen wurde eine Vielzahl von Produktkategorien erfolgreich auf das MDR Zertifikat aufgenommen.
Die jeweiligen EU Zertifikate gemäß MDR, die von der benannten Stelle ausgestellt wurden, werden jeweils um die entsprechenden Produktkategorien erweitert.
Wann werden alle betroffenen Produkte von Fresenius Medical Care den neuen MDR-Anforderungen entsprechen?
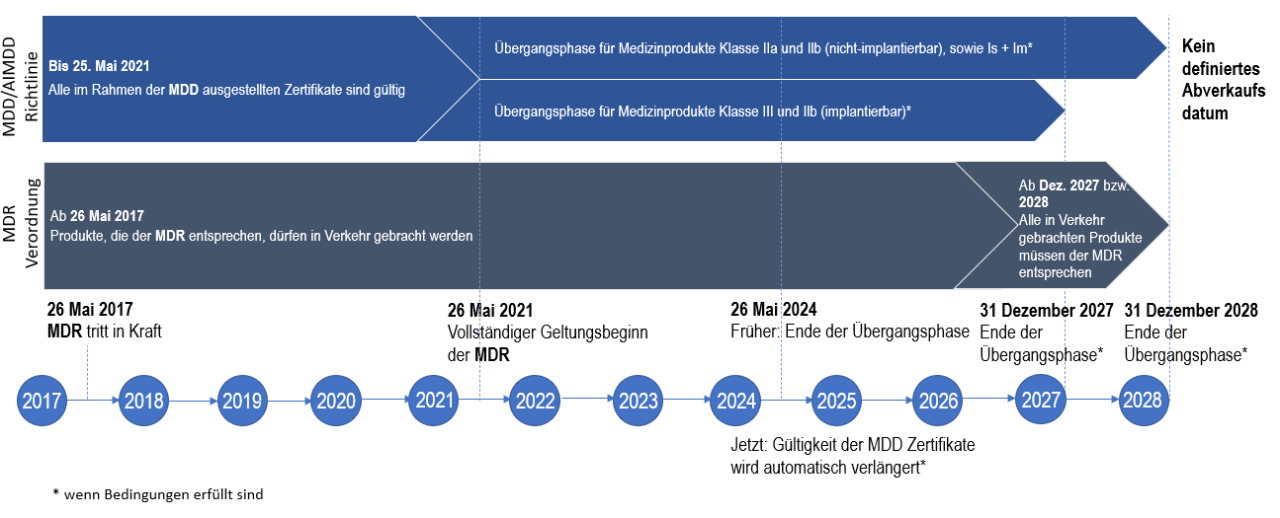
Unsere Medizinprodukte werden während der gesetzlich festgelegten Übergangsfristen von der ehemaligen MDD zur MDR im Einklang mit den geltenden EU-Anforderungen in der EU in Verkehr gebracht.
Bis Dezember 2027 bzw. Dezember 2028 (abhängig von der Klassifizierung des Medizinprodukts) können MDD-zertifizierte Produkte unter bestimmten Bedingungen nach der vollständigen Anwendbarkeit der MDR dennoch in Verkehr gebracht werden, solange ihre EG-Bescheinigungen noch gültig sind.
Dementsprechend wird Fresenius Medical Care in diesem Zeitraum sowohl MDD- als auch MDR-zertifizierte Medizinprodukte in Verkehr bringen und bis zum Ende der jeweiligen Übergangszeit (s. MDR-Übergangsfristen) werden die Produkte von Fresenius Medical Care mit MDD-Zertifizierung schrittweise nach MDR zertifiziert. In dieser Phase können Anpassungen des FME-Portfolios erforderlich werden.
Welche Änderungen der Etikettierung sind für MDR-zertifizierte Produkte zu erwarten?
MDR-zertifizierte Produkte benötigen eine eindeutige Gerätekennung (UDI). Die UDI ist eine Reihe numerischer oder alphanumerischer Zeichen, welche die Identifizierung eines konkreten Produkts auf dem Markt erlauben.
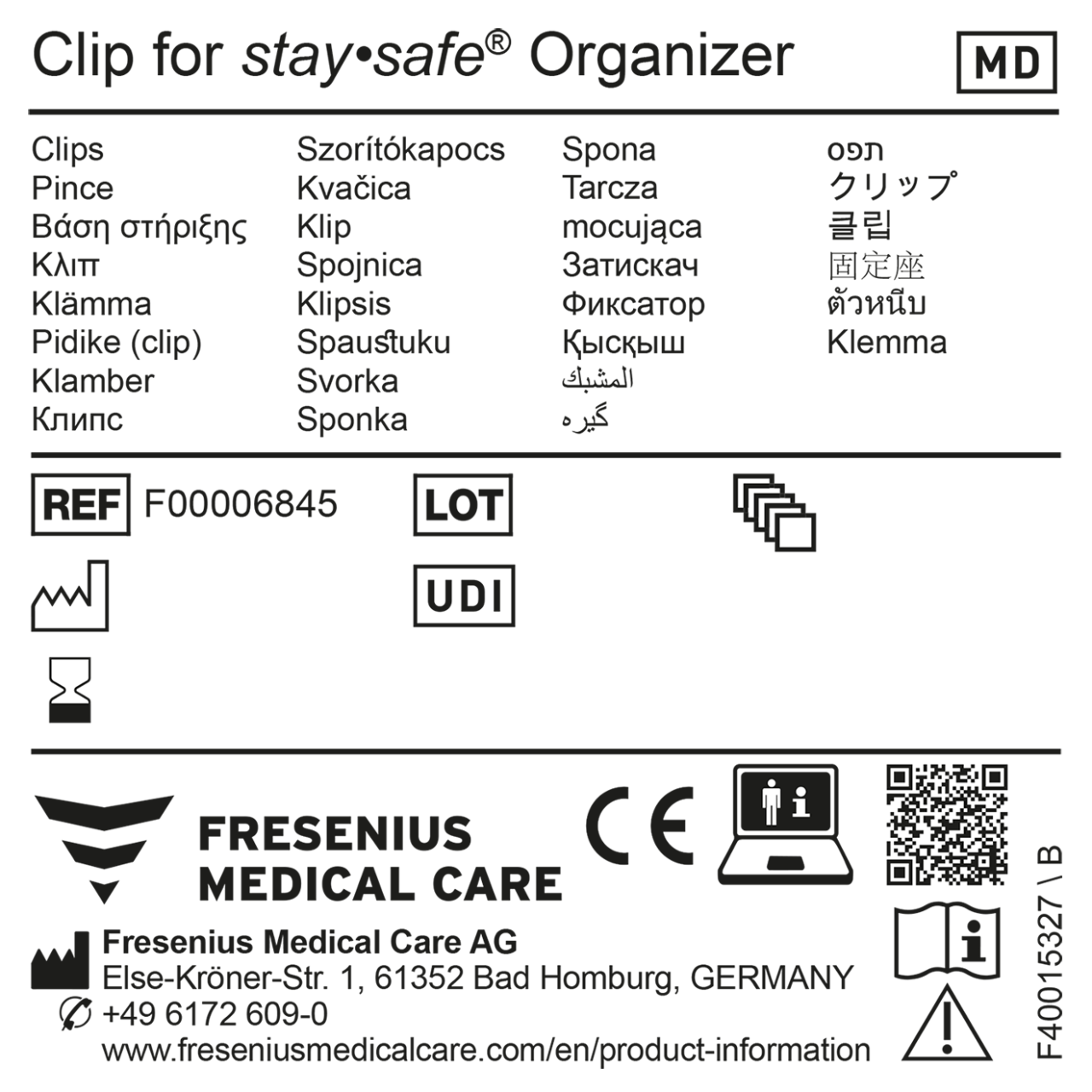
Für MDR-zertifizierte Produkte sind spezifische Symbole zu verwenden, Beispiele finden Sie in der ersten Abbildung.
Die UDI-Kennung auf MDR-konformen Produkten ersetzt nicht die Artikelnummer, sondern dient vielmehr der Identifizierung und der Rückverfolgbarkeit des Produkts über seine gesamte Lebensdauer.*
In der zweiten Abbildung finden Sie ein Beispiel für ein MDR- konformes allgemeines Beispieletikett.
Welches Niveau der Rückverfolgbarkeit unserer Medizinprodukte müssen die Kunden nach Umsetzung der UDI-Etikettierungsanforderung gewährleisten?
MDR-zertifizierte Produkte benötigen eine eindeutige Gerätekennung (UDI). Die UDI ist eine Reihe numerischer oder alphanumerischer Zeichen, welche die Identifizierung eines konkreten Produkts auf dem Markt erlauben.
Zu den von Kunden zu beachtenden Pflichten hat die EU-Kommission Merkblätter veröffentlicht (siehe Abschnitt Links unten*).
Eindeutige Gerätekennung (UDI)
Bevollmächtigte Vertreter, Händler und Importeure
Medizinisches Fachpersonal und Gesundheitseinrichtungen
Worin liegt die Bedeutung der EUDAMED-Datenbank?
Die Europäische Datenbank für Medizinprodukte (EUDAMED) ist eine von der EU-Kommission verwaltete Datenbank zur Speicherung von Informationen über Medizinprodukte.
Ziel von EUDAMED ist es, die Marktüberwachung zu stärken, indem den zuständigen Behörden ein schneller Zugang zu Informationen über Hersteller, bevollmächtigte Vertreter, Medizinprodukte, Zertifikate und Vigilanzdaten ermöglicht wird, Informationen über Daten aus klinischen Prüfungen auszutauschen sowie zu einer einheitlichen Anwendung der regulatorischen Anforderungen beizutragen, insbesondere in Bezug auf die Registrierungsanforderungen.
Alle Hersteller und alle Medizinprodukte, die in der EU in Verkehr gebracht werden sollen, werden in EUDAMED registriert. Hersteller (wie Fresenius Medical Care) müssen sicherstellen, dass alle an EUDAMED übermittelten Daten korrekt und aktuell sind. Zu den Daten gehören produktbezogene Daten, Daten aus verschiedenen Marktüberwachungsberichten und Daten über den registrierten Wirtschaftsakteur.
Fresenius Medical Care wird weiterhin dafür Sorge tragen, die Anforderungen hinsichtlich der EUDAMED-Registrierung und der Berichterstattung gemäß den gesetzlich festgelegten Fristen zu erfüllen.